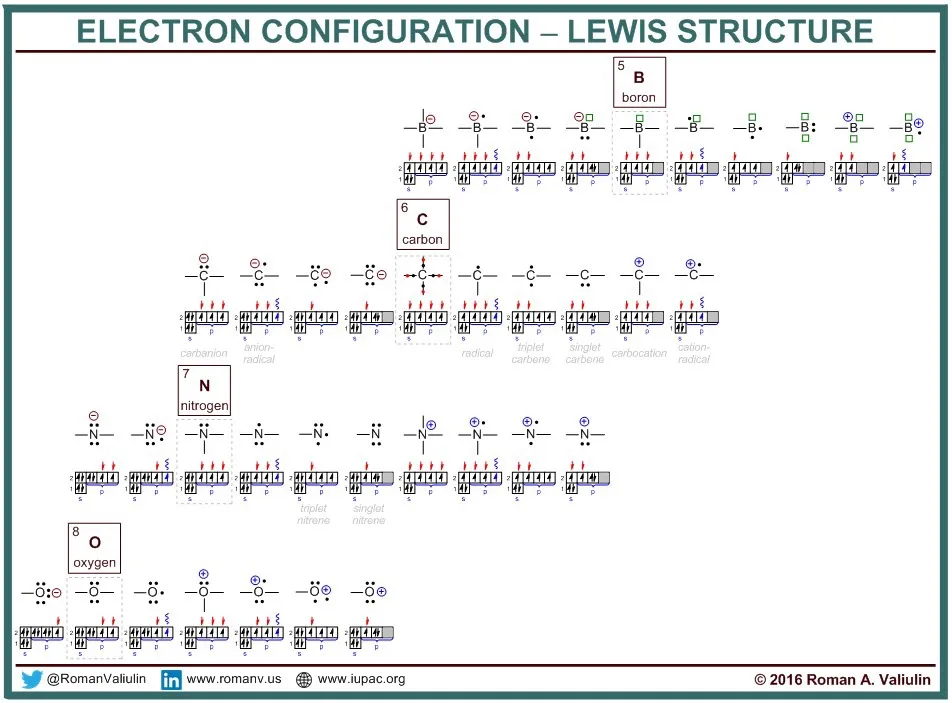
图片来源:https://cheminfographic.wordpress.com/2016/12/21/lewis-dot-structure/
路易斯结构
1916年美国物理化学家吉尔伯特·路易斯(Gilbert N. Lewis)提出了共价学说,建立了经典的共价键理论。此理论的核心是原子间通过共用电子对形成最外层8电子的稳定结构(ns2np6)(氢除外),故路易斯价健理论又称八隅体理论。该理论适用于绝大多数主族元素的共价化合物和含共价键的离子,而路易斯结构式的表示要求是:用短线表示原子间形成的共价键,同时用小黑点表示未用于形成共价键的电子(非键合电子),也可省去这些小黑点。
A、B 两原子各有一个成单电子,当 A、B 相互接近时,两电子以自旋相反的方式结成电子对,即两个电子所在的原子轨道能相互重叠,则体系能量降低,形成化学键,亦即一对电子则形成一个共价键。
形成的共价键越多,则体系能量越低,形成的分子越稳定。因此,各原子中的未成对电子尽可能多地形成共价键。
配位键形成条件:一种原子中有孤对电子,而另一原子中有可与孤对电子所在轨道相互重叠的空轨道。在配位化合物中,经常见到配位键。
该理论适用于绝大多数主族元素的共价化合物和含共价键的离子,而路易斯结构式的表示要求是:用短线表示原子间形成的共价键,同时用小黑点表示未用于形成共价键的电子(非键合电子),也可省去这些小黑点。这里应注意:非键合电子可以是成对的(孤对电子),也可以是成单的(自由基中)。