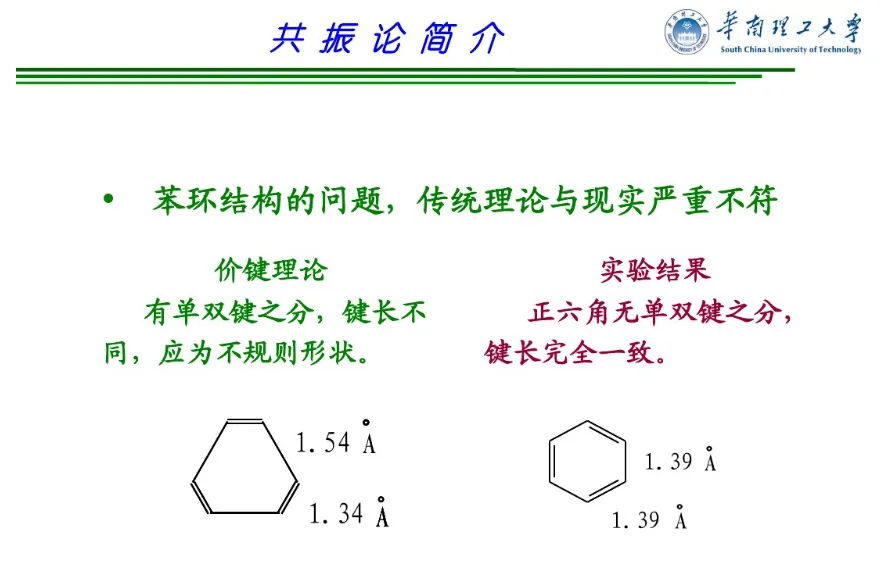
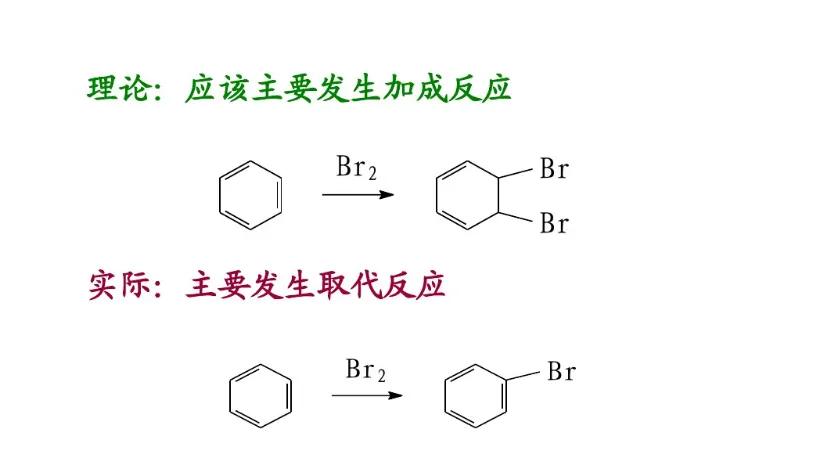
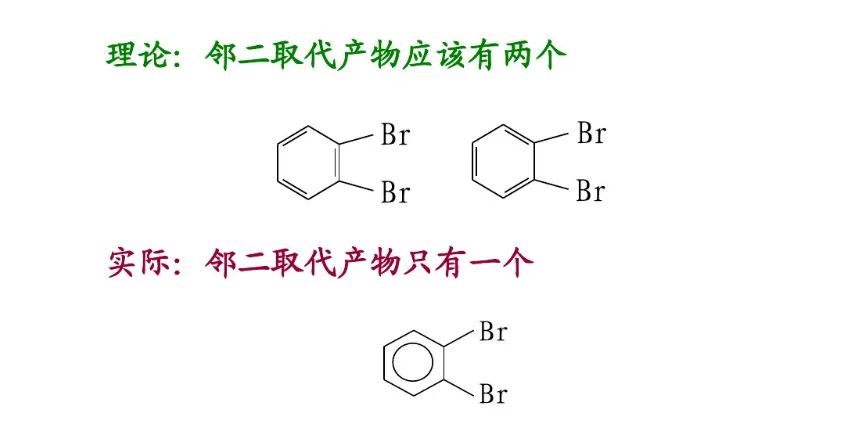
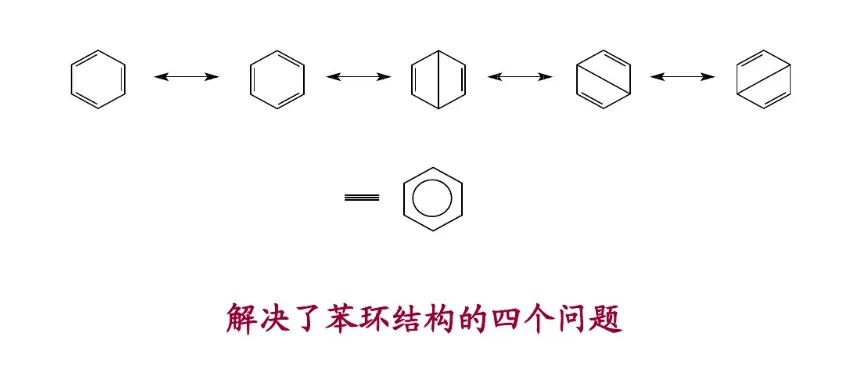
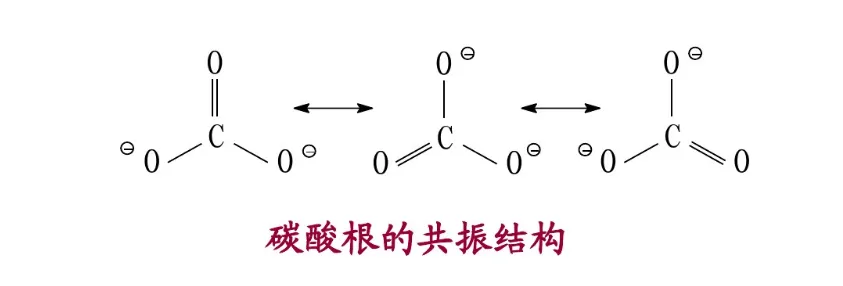
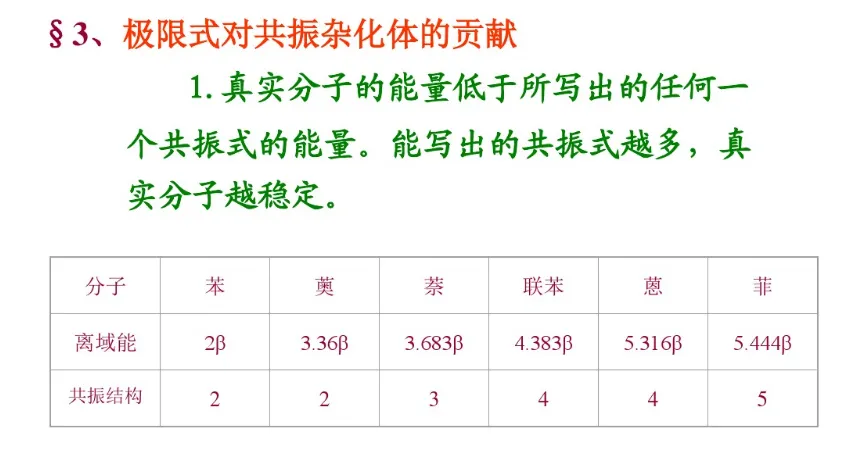
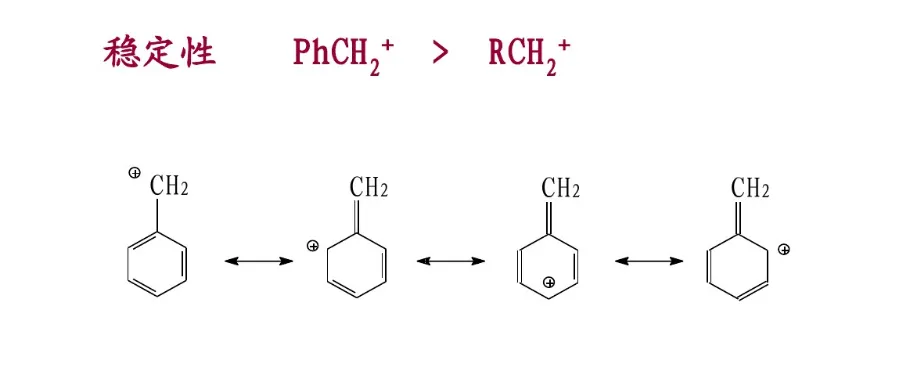
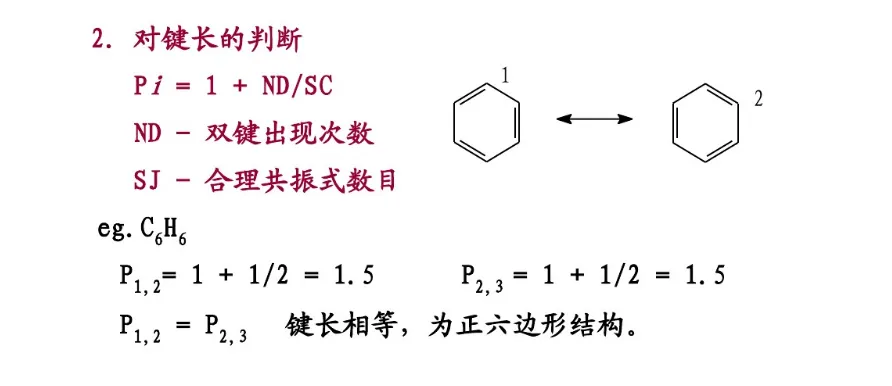
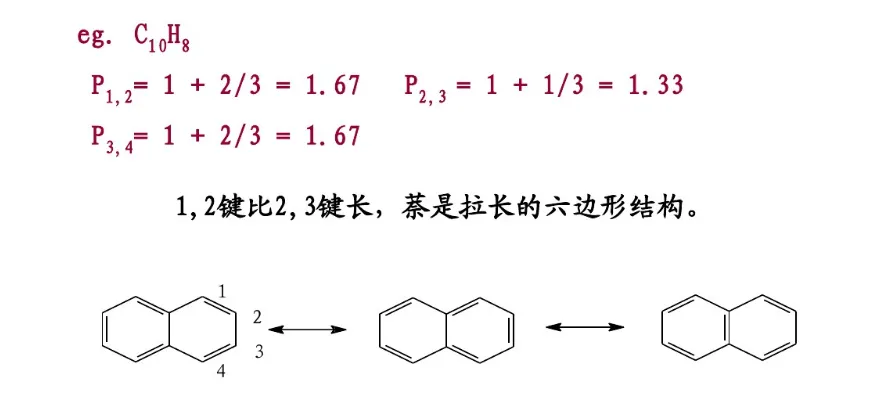
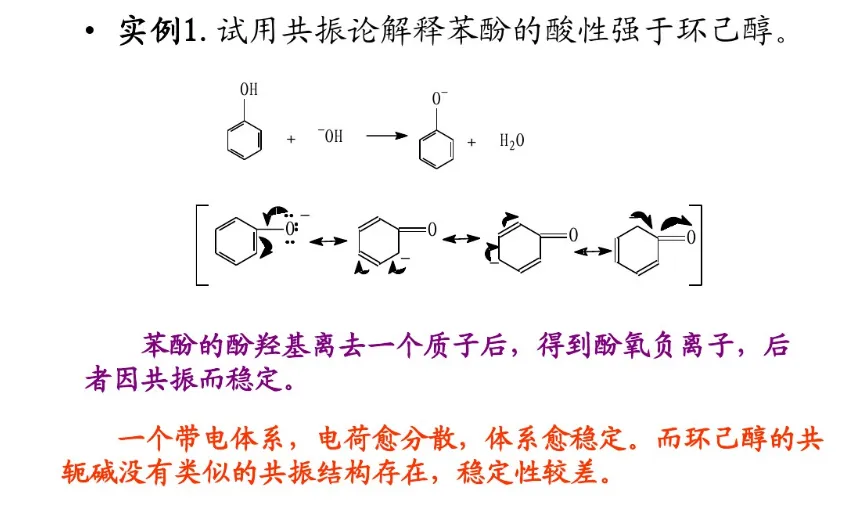
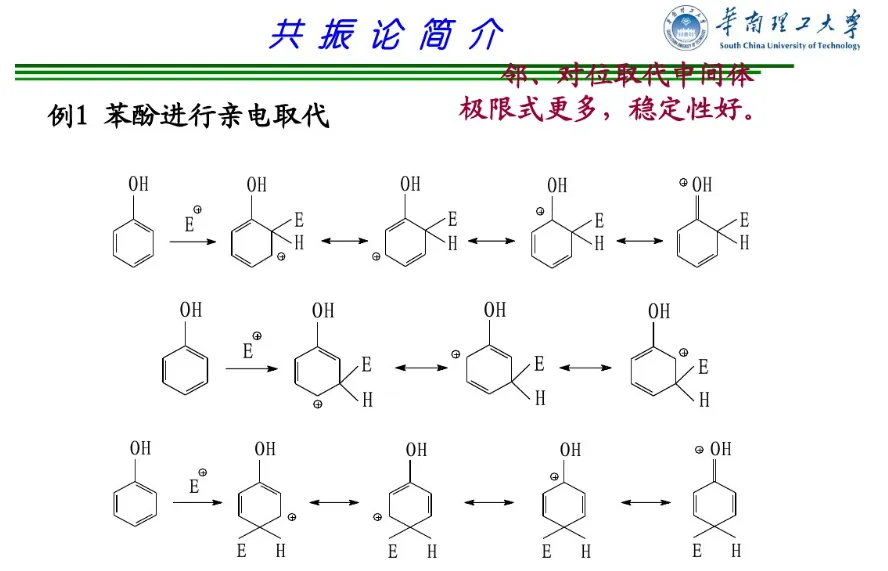
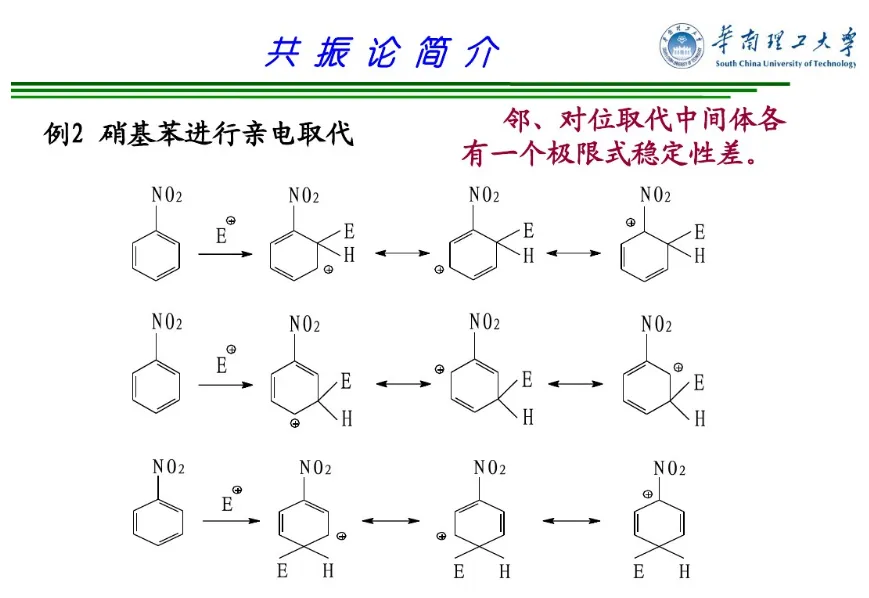
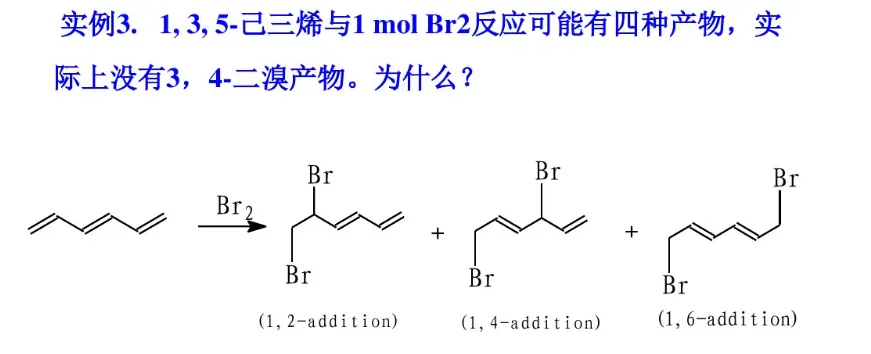
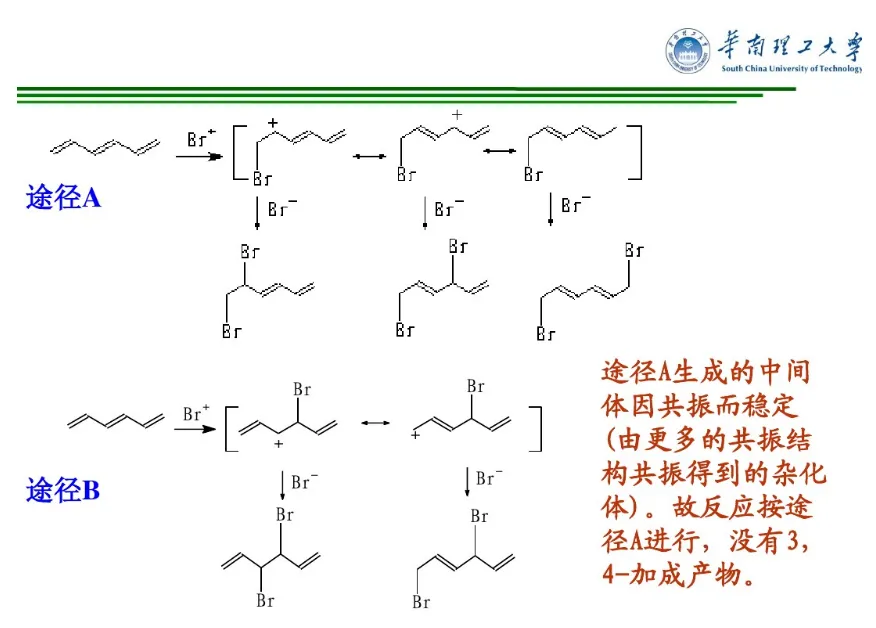
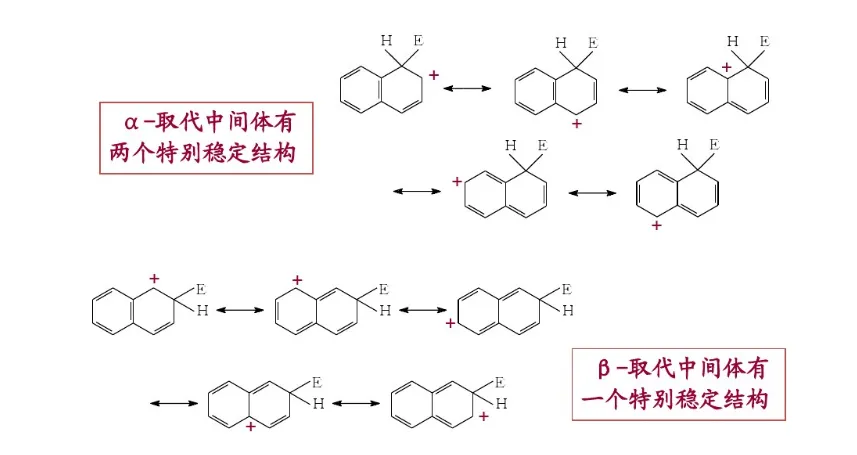
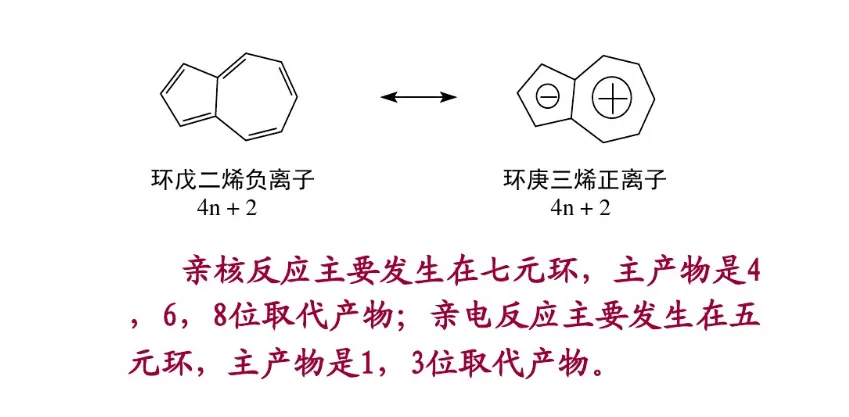
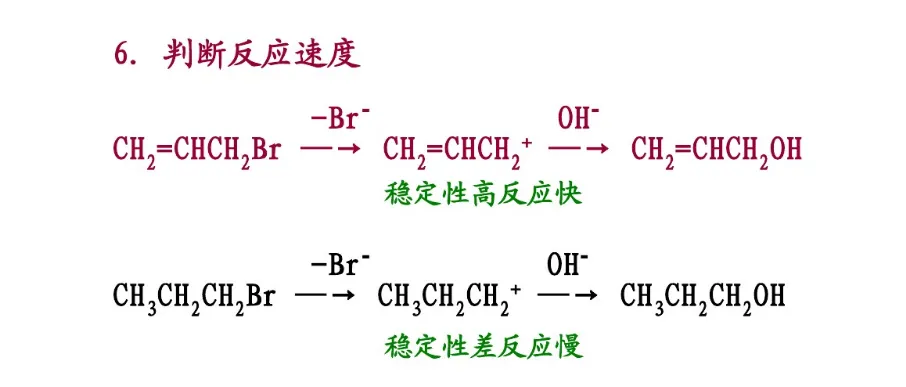
共振论是1931年鲍林(L. C. Pauling)创立的一种分子结构理论。当一个分子、离子或自由基的结构不能用路易斯结构式(Lewis structure)正确地描述时,可以用多个路易斯式表示,这些路易斯式称为共振结构(resonance structure,又称共振式或极限式)。在共振结构之间用双箭头“←→”联系,以表示它们的共振关系。例如苯分子是由下述共振结构参与共振的,但任何一个共振结构都不足以反映分子的真实结构,实际上,苯没有单双键之分,键长都为0.139nm,其邻二取代物只有一种,而且苯具有特殊的稳定性,典型的化学反应不是烯烃的加成反应,而是取代反应。
共振极限式是共振分子在参与共振过程中到达的一种极限状态,实际中并不能稳定单独存在。
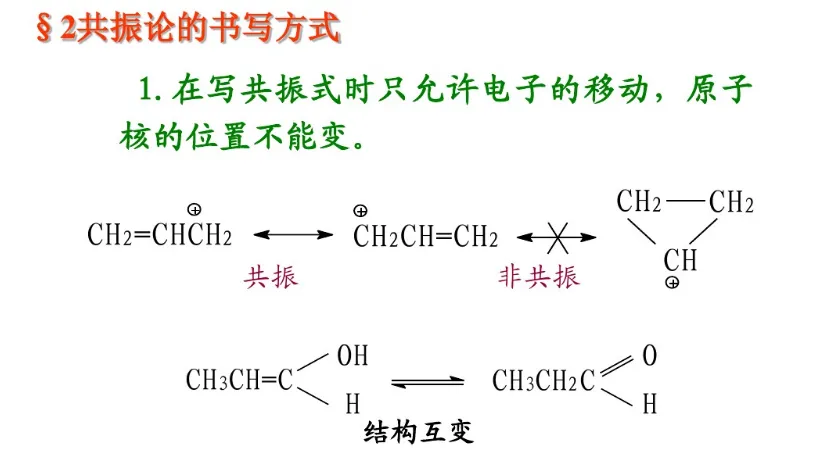
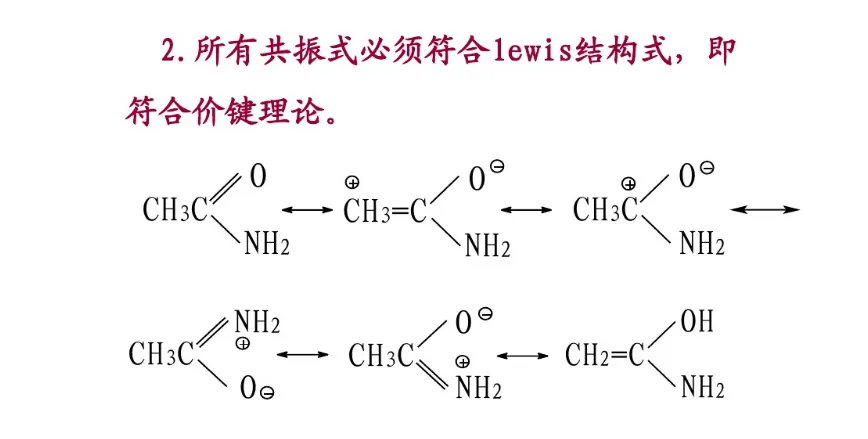
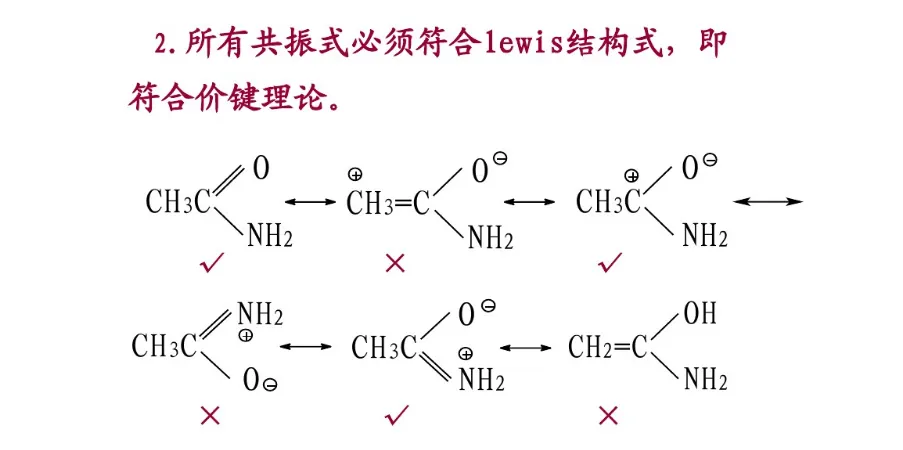
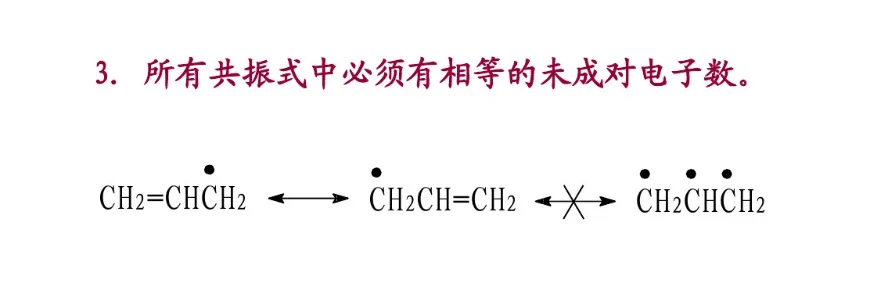
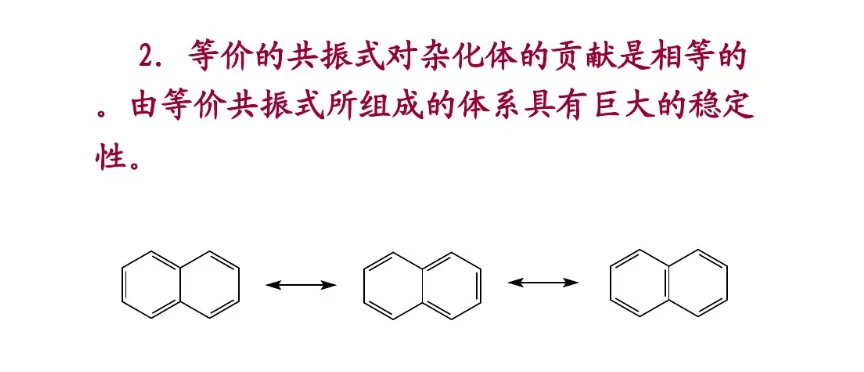
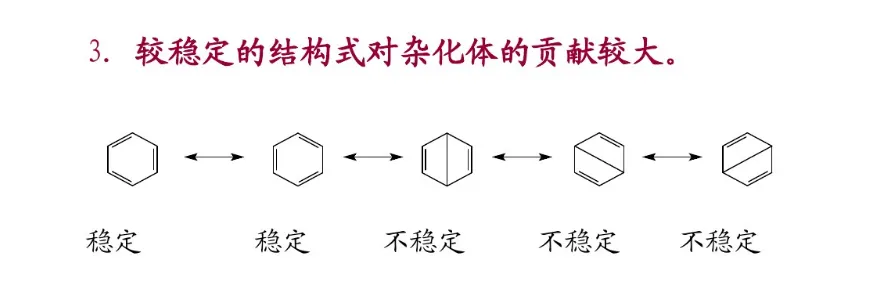
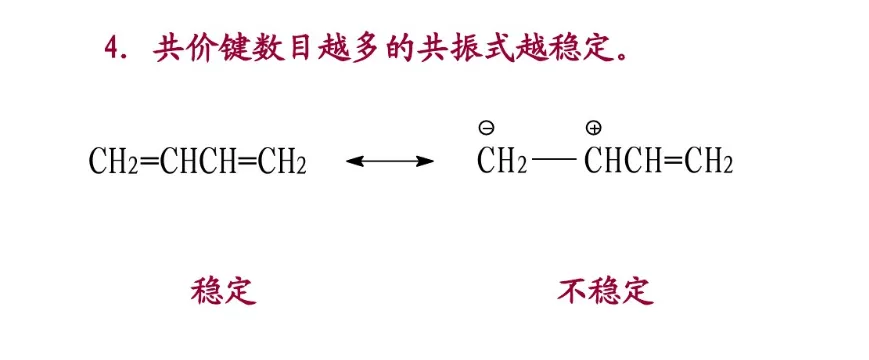
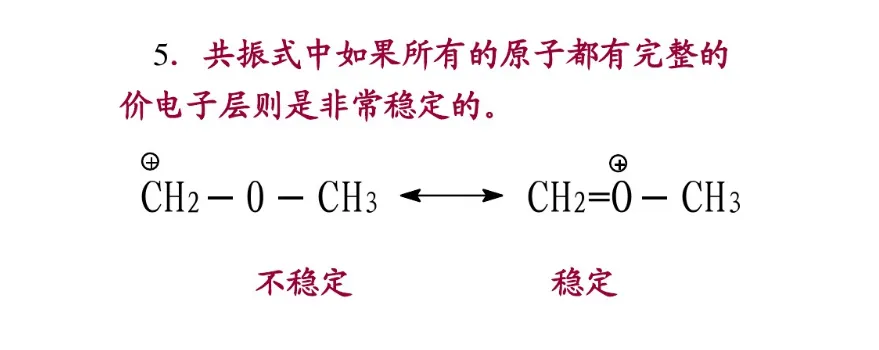
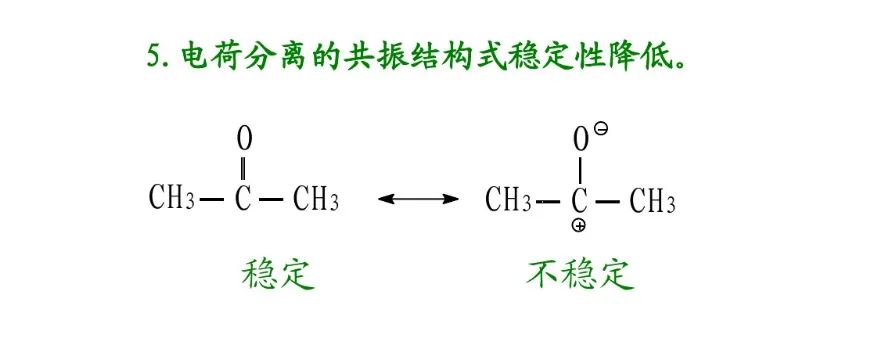
分子的真实结构是这些共振结构共振得到的共振杂化体(resonance hybrid)。杂化体既不是极限结构的混合物,也不是它们的平衡体系,而是一个具有确定结构的单一体,它不能用任何一个极限结构来代替。每个共振结构对共振杂化体的贡献不同,即它们对共振杂化体的参与程度有差别。共振结构越稳定,对共振杂化体的贡献越大。共振结构的书写除符合价键规则外,还必须遵守各共振结构的原子核位置不变,各共振结构的配对电子数或未共享电子数不变的原则。
有关共振论几点争议:
一、共振论不能解释化合物的芳香性【详见休克尔规则(Hückel规则)】,有时会得到相反的结论。
二、参与共振的极限结构不是真实存在的。
三、共振论假定分子是非激发态结构的共振杂化体,因此无法解释反应过程中的激发态问题。
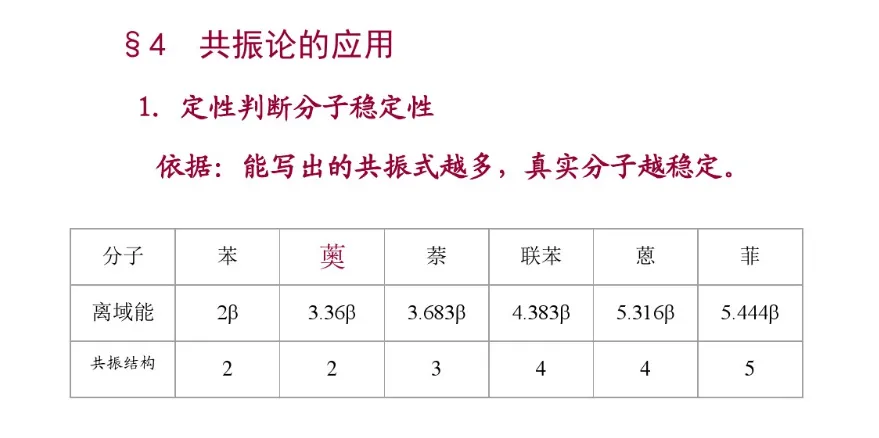
四、“分子参加共振的数目越多,分子就越稳定”的规则具有很大的任意性。
本文转自:
一、百度百科https://baike.baidu.com/item/%E5%85%B1%E6%8C%AF%E6%9E%81%E9%99%90%E5%BC%8F/19426491?fr=aladdin
二、https://wenku.baidu.com/view/4529666708a1284ac950439b.html
三、基础有机化学;第四版,上册,p402.